MateriKimia Bilangan Kuantum Spin
Bilangan kuantum terakhir yang sobat Materi Kimia SMA adalah bilangan kuantum spin. Bilangan kuantum ini ditemukan dari hasil
pengamatan radiasi uap perak yang dilewatkan melalui medan magnet, oleh Otto
Stern dan W. Gerlach.
Pada medan magnet, berkas
cahaya dari uap atom perak terurai
menjadi dua berkas. Satu berkas membelok ke kutub utara magnet dan satu berkas
lagi ke kutub selatan magnet. Berdasarkan pengamatan tersebut, disimpulkan
bahwa atom-atom perak memiliki sifat magnet.
Pengamatan terhadap
atom-atom unsur lain, seperti atom Li, Na, Cu, dan Au selalu menghasilkan
gejala yang serupa. Atom-atom tersebut memiliki jumlah elektron ganjil.
Munculnya sifat magnet dari berkas uap atom disebabkan oleh spin atau putaran
elektron pada porosnya.
Berdasarkan percobaan
Stern-Gerlach, dapat disimpulkan bahwa ada dua macam spin elektron yang
berlawanan arah dan saling meniadakan. Pada atom yang jumlah elektronnya
ganjil, terdapat sebuah elektron yang spinnya tidak ada yang meniadakan.
Akibatnya, atom tersebut memiliki medan magnet.
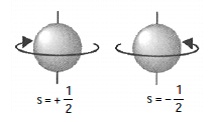
Spin elektron dinyatakan
dengan bilangan kuantum spin. Bilangan kuantum ini memiliki dua harga yang
berlawanan tanda, yaitu +½ dan –½. Tanda (+) menunjukkan putaran searah jarum
jam dan tanda (–) arah sebaliknya. Adapun harga ½ menunjukan fraksi elektron.
Setelah bilangan kuantum, materi
kimia kelas XI yang akan sobat Materi
Kimia SMA pelajari adalah bentuk
orbital












 9/18/2013 10:07:00 PM
9/18/2013 10:07:00 PM
 simbah wuri
simbah wuri


 Posted in:
Posted in: 








0 komentar:
Posting Komentar
Akan bijak bila memberi komentar bukan spam